我们常常在电视上看到许多肿瘤科医生的采访视频中会出现“免疫治疗”这几个字,这种新型的治疗方式有望成为继“手术”“放疗”“化疗”之后的第四种有效的抗癌策略。而免疫治疗中“出力”最多的就是我们体内可爱的免疫细胞。其中包括NK细胞,T细胞,DC细胞在内在各个领域散发着光芒!
DC细胞是什么?
1973年Steiman和Cohn首次从脾脏中分离出一类与粒细胞、巨噬细胞和淋巴细胞形态和功都不同的白细胞,因其细胞膜向外伸出,形成与神经细胞轴突相似的膜性树状突起,故而命名为树突状细胞。
它是机体功能最强的专职抗原递呈细胞(Antigen presenting cells, APC),它能高效地摄取、加工处理和递呈抗原,未成熟DC具有较强的迁移能力,成熟DC能有效激活初始型T细胞,处于启动、调控、并维持免疫应答的中心环节。
DC与肿瘤的发生、发展有着密切关系,大部分实体瘤内浸润的DC数量多则患者预后好。有效的抗肿瘤免疫反应的核心是产生以CD8+ T细胞为主体的细胞免疫应答,这也是DC作为免疫治疗手段的基础。
美国杜克大学遗传和细胞治疗学中心的研究主任埃利-吉尔波瓦说过:“DC是激发机体免疫系统激发抵御癌症侵袭最有效的途径之一。”“DC作为高度专职化的主要抗原递呈细胞,在诱导针对相关抗原的高效、特异性T细胞免疫应答中起到关键作用。”
DC细胞能力出众的秘诀就在于,它既可“抓捕”异常细胞(比如癌细胞)还有病毒,杀伤病原体感染的宿主细胞。也可以“捕获”关于癌症的“特征碎片”将信息传递给杀手T细胞。(DC可以快速找到抗原,将信息传递给辅助性T细胞)。
因为表面具有星状多形型或树枝状突起,被称为树突状细胞,在细胞免疫应答的过程中它也是非常重要的一环。
DC细胞的发现是被一位医学科学家斯坦曼教授的发现的,不仅如此在教授罹患癌中之王“胰腺癌”时,发挥了疗效,教授利用自身的DC疫苗,拯救自己,并延长了生存期达4年。用科学拯救自己,用DC细胞抗癌!
来源
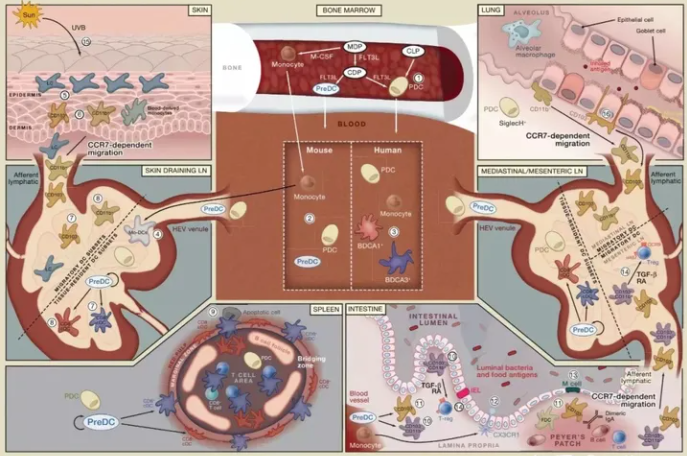
人树突状细胞起源于造血干细胞(hemopoieticstemcell)。DC的来源有两条途径:
①髓样干细胞在GM-CSF的刺激下分化为DC,称为髓样DC(myeloid dendritic cells,MDC),也称DCl,与单核细胞和粒细胞有共同的前体细胞;包括朗格汉斯细胞(Langerhans cells ,LCs),间皮(或真皮)DCs以及单核细胞衍生的DCs等。
②来源于淋巴样干细胞,称为淋巴样DC(Lymophoid dendritic cells,LDC)或浆细胞样DC(plasmacytoid dendritic cells,piX;),即DC2,与T细胞和NK细胞有共同的前体细胞。树突状细胞(DC)尽管数量不足外周血单核细胞的1%,但表面具有丰富的抗原递呈分子(MHC-Ⅰ和MHC-Ⅱ)、共刺激因子(CD80/B7-1、CD86/B7-2、CD40、CD40L等)和粘附因子(ICAM-1、ICAM-2、ICAM-3、LFA-1、LFA-3等),是功能强大的专职抗原递呈细胞(APC)。
DC自身具有免疫刺激能力,是惟一能激活未致敏的初始型T细胞的APC。
肺癌
在使用个性化新抗原疫苗DC疫苗治疗晚期(难治性非小细胞肺癌)癌症(NCT02956551)的初步临床试验研究中,结果显示目标有效率为25%,疾病控制率为75%,中位无进展生存期(PFS)为5.5个月,中位OS(总生存期)为7.9个月。而另一项关于复发性的小细胞肺癌患者中接种了TP53(一种基因)转染的DC疫苗(Ad.p53-DC)的随机对照II期试验表明DC疫苗是安全的,不同实验组的阳性免疫应答率在20%至43.3%之间。尽管该疫苗未能提高二线化疗的ORR(客观缓解率),但其安全性和治疗免疫潜力仍然存在。
黑色素瘤
2023ASCO上发表了一篇:淋巴结内注射肽脉冲成熟树突状细胞疫苗可使黑色素瘤患者具有卓越的 CD8 T 细胞功能+
CD8+T细胞是T淋巴细胞的1个亚群,CD8淋巴细胞可以分化为细胞毒性T淋巴细胞,这是可以抵制外来病原体的入侵,包括各种病毒的入侵可以杀灭外来的病原体,因此是有一定保护作用的。
临床研究数据
此项研究旨在评估通过不同途径给药的成熟肽脉冲树突状细胞(DC)疫苗的可行性、安全性和免疫原性。
对27名接受四种自体肽脉冲DC疫苗接种的转移性黑色素瘤患者进行了一项随机的I期剂量递增研究:患者被随机分配到静脉(IV)、淋巴结内(IN)或皮内(ID)给药途径(ROA)。
结果表示:27名患者中有22人(81.5%)完成了全部4次疫苗接种。疫苗接种耐受性良好;所有给药途径都诱导了四聚体染色的CD8 T细胞的类似增加。淋巴结内(IN)途径诱导CD8 T细胞的新生发展率显著更高.
由上述的临床实验数据我们发现通过IN、IV或ID途径给药该肽脉冲成熟DC疫苗是可行和安全的。
急性髓系淋巴细胞白血病
2023年7月28日在知名期刊《Leukemia》发表了一篇关于树突状疫苗与急性髓系白血病之间的临床研究,题目叫做:WT1和PRAME RNA负载的树突状细胞疫苗作为强化诱导化疗后新发AML的维持治疗
名字有点拗口,我们来一一分析。
诱导化疗:诱导化疗又称新辅助化疗,可在短时期内减少肿瘤负荷并减轻由于肿瘤引起的各种临床症状,对亚临床转移灶也有一定的作用,常用含铂类的化疗方案。
而WT1和PRAME是肾母细胞瘤基因(WT1)、黑色素瘤优先表达抗原(PRAME)。
WT1基因是从肾母细胞瘤(Wilms 瘤)染色体11p13上分离出来的肿瘤基因。近二十年的大量研究表明,虽然正常人中难以检测到 WT1的表达但在几乎所有白血病患者中能检测到,其敏感度也较高。
20名首次CR(CR1)不符合allo-HSCT条件的AML患者接受了FDC101治疗,FDC101是一种表达两种白血病相关抗原(LAA)的自体RNA负载成熟树突状细胞(mDC)疫苗。治疗耐受性良好,有轻微和短暂的注射部位反应。20名患者中有11名(55%)仍处于CR状态,而6名复发患者中有4名在抢救治疗后达到CR2,并接受了同种异体造血干细胞移植。五年时OS为75%,70%≥60岁的患者为长期幸存者。这种DC疫苗的维持治疗在CR1的AML患者中具有良好的耐受性,并伴有令人鼓舞的5年长期生存率。

