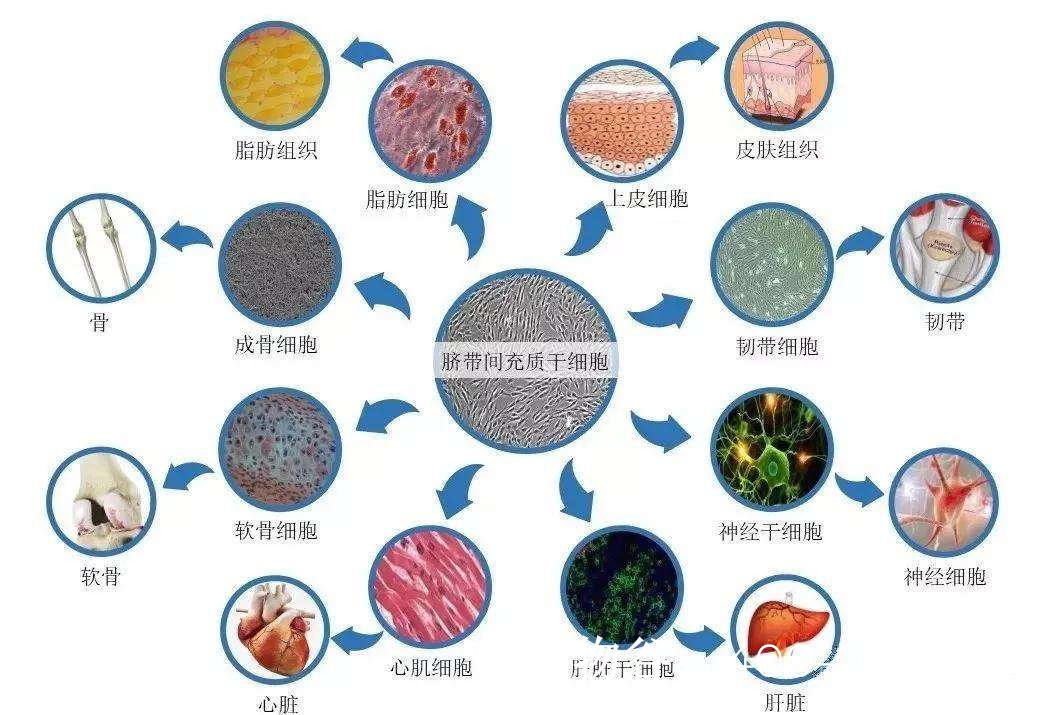
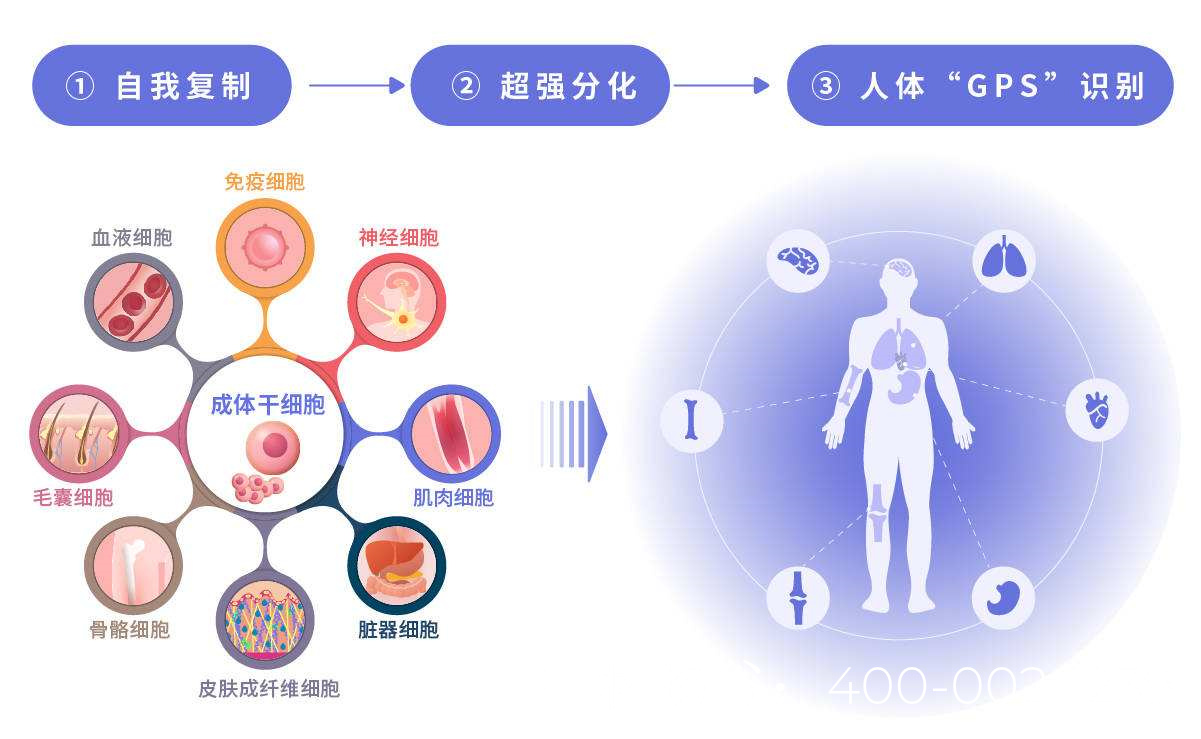
干细胞修复卵巢早衰的原理是什么
卵巢早衰(Premature Ovarian Failure, POF)是指女性在40岁之前出现卵巢功能衰退,表现为闭经、雌激素水平降低和不孕等症状。传统治疗方法如激素替代疗法(HRT)虽能缓解症状,但无法从根本上恢复卵巢功能。近年来,干细胞疗法因其强大的再生和修复能力,成为卵巢早衰治疗的研究热点。本文将探讨干细胞修复卵巢早衰的作用机制及其临床应用前景。
干细胞修复卵巢早衰的机制
1. 促进卵泡再生
卵巢早衰的主要病理特征是卵泡数量减少或功能丧失。干细胞(如间充质干细胞MSCs、胚胎干细胞ESCs、诱导多能干细胞iPSCs等)可通过以下方式促进卵泡再生:
分化为**或颗粒细胞:研究表明,干细胞在特定微环境下可分化为卵泡细胞,补充受损的卵泡池。
分泌生长因子:干细胞可分泌血管内皮生长因子(VEGF)、胰岛素样生长因子(IGF-1)等,促进卵泡发育和成熟。
2. 改善卵巢微环境
卵巢功能的维持依赖于健康的微环境,包括血管网络、免疫调节和细胞外基质的支持。干细胞通过以下方式改善卵巢微环境:
促进血管生成:干细胞分泌的VEGF等因子可刺激血管新生,改善卵巢血流,增强营养供应。
调节免疫反应:卵巢早衰常伴随炎症和自身免疫反应,干细胞可通过调节T细胞、巨噬细胞等免疫细胞功能,减少卵巢损伤。
3. 抗凋亡与抗氧化作用
氧化应激和细胞凋亡是卵巢早衰的重要诱因。干细胞可通过以下途径保护卵巢细胞:
减少活性氧(ROS)积累:干细胞分泌的超氧化物歧化酶(SOD)、谷胱甘肽过氧化物酶(GPx)等抗氧化酶可减轻氧化损伤。
抑制凋亡信号通路:干细胞能下调促凋亡蛋白(如Bax、Caspase-3),上调抗凋亡蛋白(如Bcl-2),提高卵泡存活率。
4. 旁分泌效应
干细胞不仅通过直接分化发挥作用,还能通过旁分泌机制释放外泌体(Exosomes),其中包含微小RNA(miRNA)、蛋白质和细胞因子,调控卵巢细胞的增殖、分化和修复。
干细胞来源及临床应用研究
目前用于卵巢早衰治疗的干细胞主要包括:
间充质干细胞(MSCs):来源于骨髓、脂肪、脐带等,具有低免疫原性和易获取的特点,是研究最广泛的干细胞类型。
胚胎干细胞(ESCs)和诱导多能干细胞(iPSCs):具有更强的分化潜能,但存在伦理和安全性问题,目前仍处于实验阶段。
卵巢干细胞(OSCs):近年研究发现卵巢中存在具有自我更新能力的干细胞,可能为卵巢修复提供新途径。
临床研究进展
动物实验:多项研究表明,干细胞移植可恢复卵巢早衰小鼠的激素水平,促进卵泡形成,甚至成功受孕。
临床试验:已有小规模临床研究显示,干细胞移植可部分恢复POF患者的月经周期和激素水平,但长期疗效和安全性仍需进一步验证。
结论
干细胞通过多途径(分化、旁分泌、免疫调节等)修复受损卵巢,为卵巢早衰患者带来新希望。随着研究的深入,干细胞疗法有望成为恢复卵巢功能、提高生育能力的有效方法。