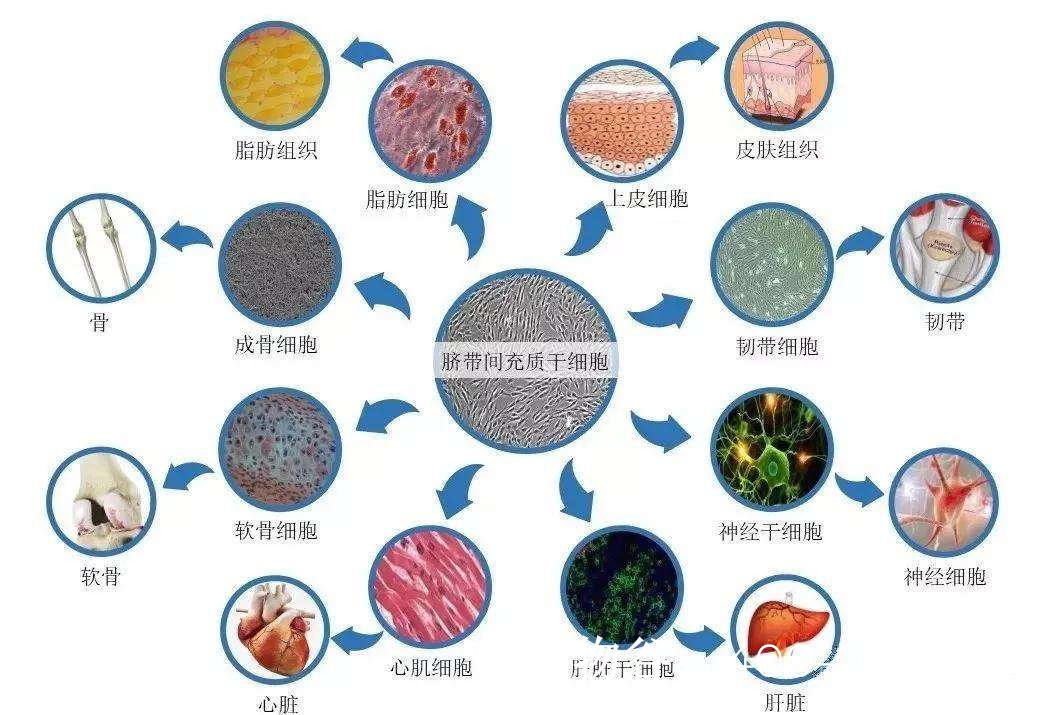
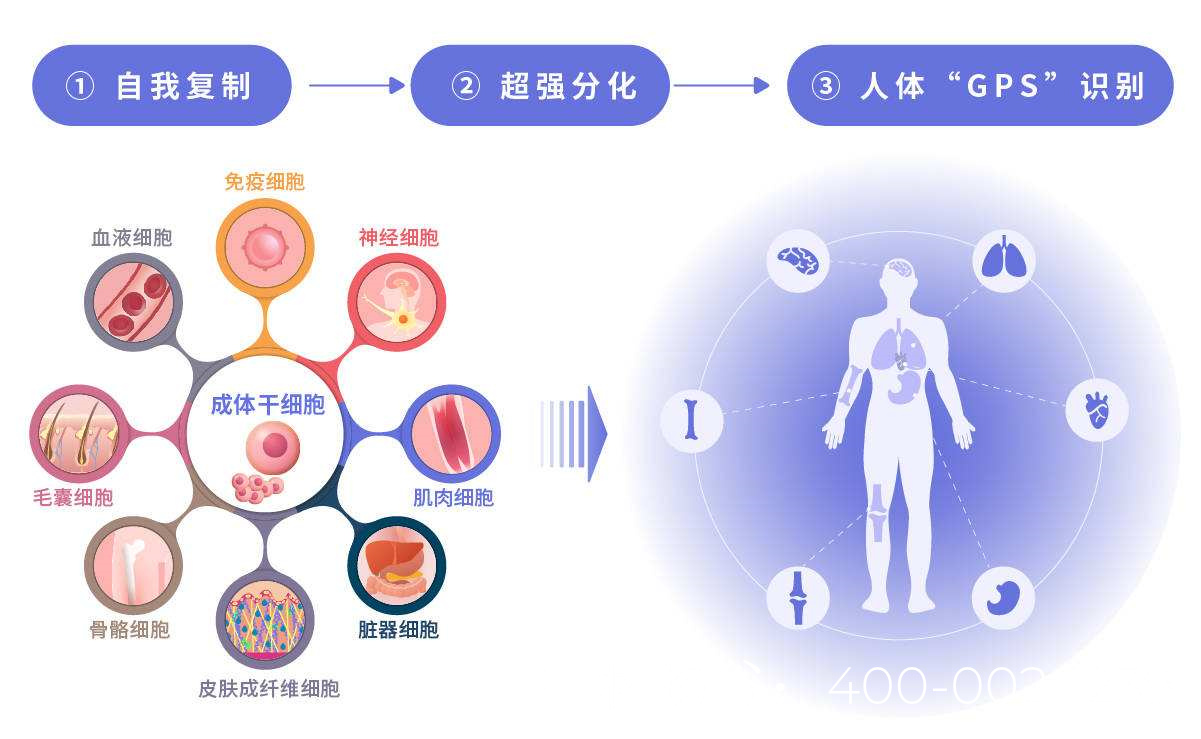
没有生精细胞干细胞还能治疗吗?
男性不育症中,无精症(azoospermia)是最严重的一种,其中部分患者睾丸活检显示缺乏生精细胞(spermatogonial stem cells, SSCs),这意味着睾丸无法自然产生精子。传统观念认为,这类患者几乎无法通过自身精子生育后代,但随着干细胞技术和生殖医学的发展,科学家正在探索新的治疗途径。本文将探讨在缺乏生精细胞的情况下,干细胞治疗的可行性、研究进展及未来方向。
1. 生精细胞缺失的原因与诊断
生精细胞缺失通常由先天性因素(如克氏综合征、Y染色体微缺失)或后天损伤(如化疗、放疗、睾丸创伤)导致。诊断需通过睾丸活检和病理检查确认生精小管中是否存在SSCs或其他生殖细胞。若完全缺乏生精细胞,则称为“唯支持细胞综合征”(Sertoli cell-only syndrome, SCOS),自然生育可能性极低。
2. 干细胞治疗的潜在策略
即使患者自身缺乏生精细胞,干细胞技术仍可能提供解决方案,主要包括以下几类:
(1)多能干细胞分化为精子
胚胎干细胞(ESCs)或诱导多能干细胞(iPSCs)可通过体外定向分化生成精子前体细胞。近年来,科学家已成功将小鼠和人类的iPSCs分化为类精子细胞(sperm-like cells),但这些细胞的功能性和安全性仍需验证。
优势:无需依赖患者自身生精细胞。
挑战:分化效率低,且可能表观遗传异常,存在伦理争议。
(2)异体生精细胞移植
若患者仅因微环境异常导致生精细胞缺失,理论上可通过移植健康供体的SSCs恢复生精功能。
动物实验:小鼠模型中,移植的SSCs可在受体睾丸内定植并产生精子。
人类应用障碍:免疫排斥、供体来源限制及伦理问题(如后代遗传物质归属)。
(3)基因编辑与睾丸类器官
通过CRISPR等基因编辑技术修复患者体细胞的遗传缺陷,再将其转化为iPSCs并分化为SSCs。此外,睾丸类器官(3D培养的睾丸组织模型)可为精子发生提供体外微环境。
进展:2022年,日本团队利用小鼠iPSCs培育出功能性**,类似技术或可应用于精子发生。
3. 替代方案与综合管理
在干细胞技术成熟前,患者可考虑以下选择:
**人工授精(AID):使用志愿者精子实现生育。
**或第三方辅助生殖:如配偶卵子与**结合(IVF-D)。
睾丸显微取精(micro-TESE):约30%-50%的SCOS患者睾丸中仍存在局灶性生精区域,可通过显微手术提取少量精子用于试管婴儿(ICSI)。
4. 未来展望
随着单细胞测序、类器官培养等技术的进步,个性化干细胞疗法或成为可能。例如:
自体iPSCs疗法:避免免疫排斥,但需解决分化效率问题。
睾丸原位重编程:通过体内转分化技术,将体细胞直接转化为SSCs。
结语
尽管生精细胞缺失的患者目前治疗选择有限,干细胞技术正为其带来新希望。未来5-10年,随着基础研究的突破和临床试验的开展,无精症患者或能通过自体干细胞衍生精子实现生育梦想。然而,科学界仍需在技术优化、伦理规范及临床转化方面持续努力。