隐睾性无精子症的干细胞治疗咋样?
隐睾性无精子症(Cryptorchidism-associated Azoospermia)是男性不育的重要原因之一,表现为睾丸未能正常下降至阴囊,导致精子生成障碍。传统治疗方法(如手术矫正和激素治疗)对部分患者有效,但对于严重生精功能障碍的患者,恢复生育能力仍然困难。近年来,干细胞治疗为隐睾性无精子症提供了新的希望。本文将探讨干细胞治疗的机制、研究进展及未来发展方向。
1. 干细胞治疗的潜在机制
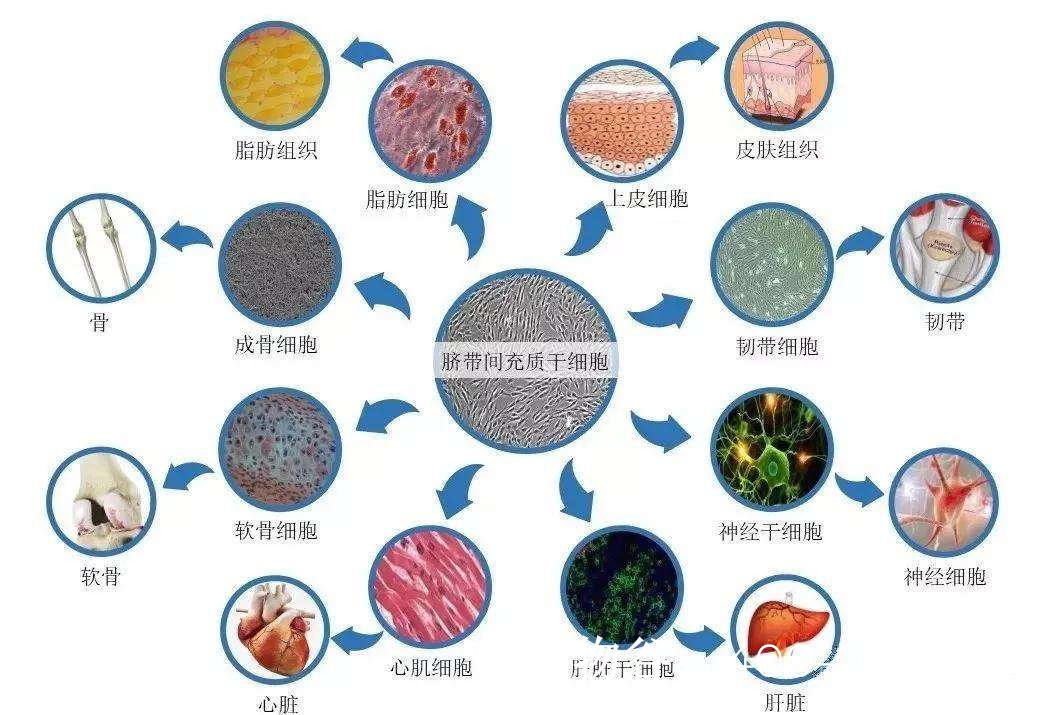
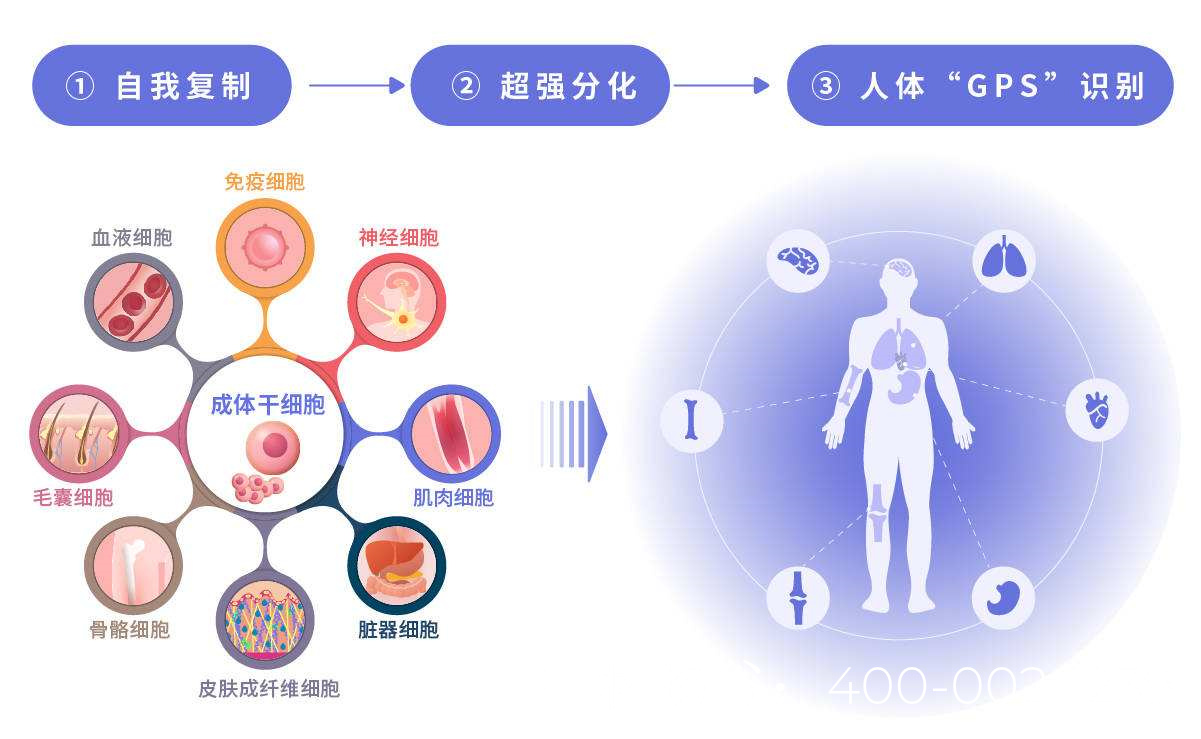
干细胞具有自我更新和分化为多种细胞类型的潜能,在修复受损组织方面具有独特优势。对于隐睾性无精子症,干细胞治疗主要通过以下途径发挥作用:
(1)促进精子发生
精原干细胞(Spermatogonial Stem Cells, SSCs)是精子生成的基础。隐睾症患者的睾丸微环境受损,SSCs数量减少或功能异常。通过移植健康的SSCs或诱导多能干细胞(iPSCs)分化为SSCs,可能恢复精子发生过程。
(2)改善睾丸微环境
隐睾症常伴随睾丸间质细胞(Leydig细胞)和支持细胞(Sertoli细胞)功能障碍,影响精子生成。间充质干细胞(MSCs)可通过旁分泌作用促进血管生成、减少炎症反应,修复受损的睾丸组织。
(3)基因修复
部分隐睾症与遗传因素(如INSL3、GREAT基因突变)相关。基因编辑技术(如CRISPR-Cas9)结合干细胞治疗,可能纠正基因缺陷,从根本上恢复生育能力。
2. 未来展望
随着再生医学的发展,干细胞治疗隐睾性无精子症可能成为现实。未来研究方向包括:
优化分化方案:提高干细胞向精原细胞分化的效率。
联合治疗:结合激素疗法、组织工程等提升疗效。
基因治疗:修复隐睾相关基因突变,从根源解决问题。
3. 结论
干细胞治疗为隐睾性无精子症患者带来了新的希望,未来需进一步探索其机制、优化技术并开展临床试验,以推动其向临床转化。对于患者而言,在现有医疗条件下,早期手术矫正和生育力保存(如精子冷冻)仍是重要选择。