干细胞治疗无精症是什么原因导致的呢
无精症(azoospermia)是男性不育的主要原因之一,指精液中完全无精子存在。传统治疗方法(如手术取精或激素治疗)效果有限,而干细胞治疗因其再生和修复潜力,成为近年来备受关注的新方向。本文将探讨干细胞治疗无精症的机制、研究进展及未来挑战。
无精症的病因及传统治疗局限
无精症可分为两大类:
梗阻性无精症(OA):输精管阻塞导致精子无法排出,但睾丸内仍有精子生成。
非梗阻性无精症(NOA):睾丸生精功能障碍,无法产生精子,占无精症的60%以上。
传统治疗方法包括:
手术取精(如TESE、Micro-TESE):适用于部分NOA患者,但成功率仅30%-50%。
激素治疗:适用于低促性腺激素性性腺功能减退症(HH),但对大多数NOA患者无效。
辅助生殖技术(ART):依赖精子提取,若无法获取精子则难以实施。
因此,干细胞治疗成为探索无精症治疗的新途径。
干细胞治疗无精症的机制
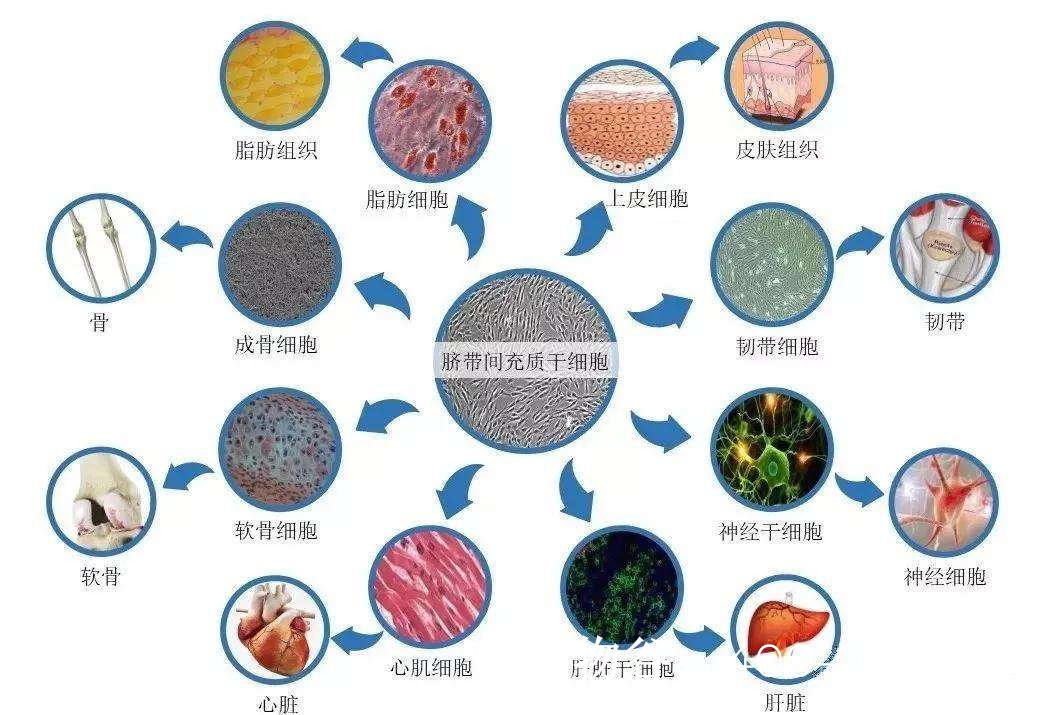
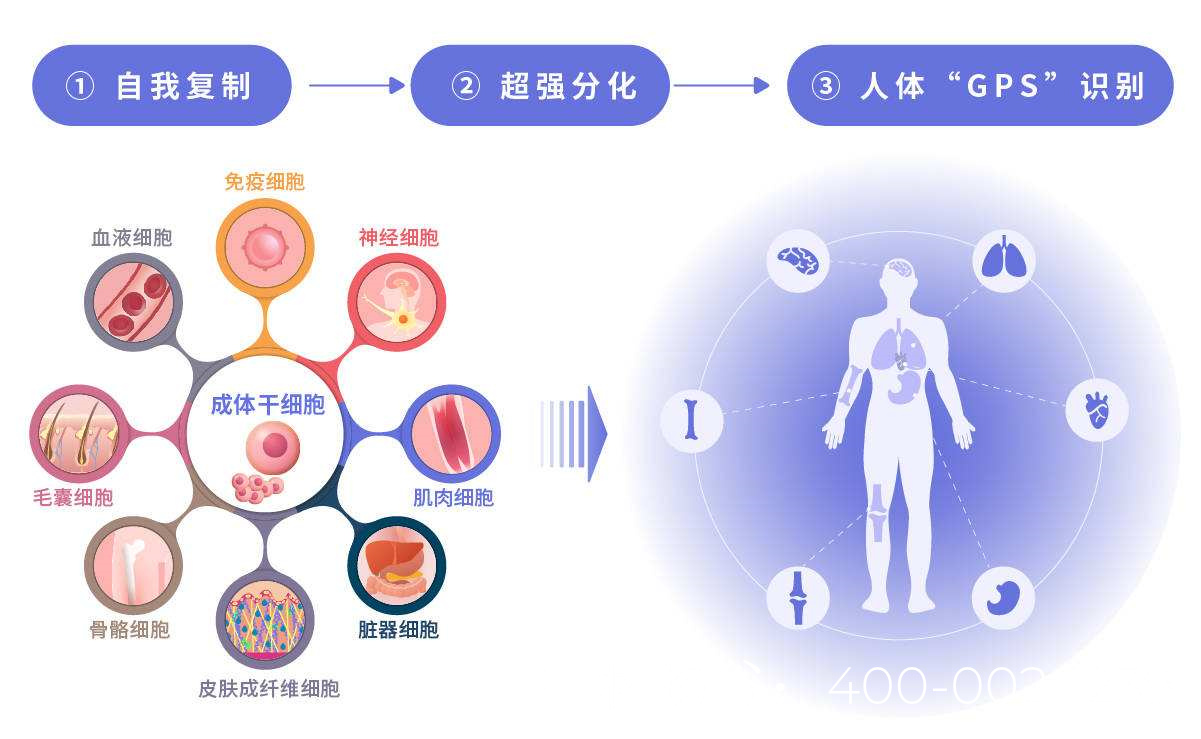
干细胞具有自我更新和分化为多种细胞类型的能力,理论上可修复或替代受损的生精细胞。其作用机制包括:
分化为精子前体细胞
胚胎干细胞(ESCs)或诱导多能干细胞(iPSCs)可在体外分化为精原干细胞(SSCs),并进一步发育为成熟精子。动物实验中,科学家已成功将小鼠干细胞转化为功能性精子,并诞生健康后代。
修复睾丸微环境
间充质干细胞(MSCs)可分泌生长因子(如GDNF、FGF2),改善睾丸支持细胞(Sertoli细胞)和间质细胞(Leydig细胞)功能,促进精子发生。
基因编辑纠正遗传缺陷
对于遗传性无精症(如Y染色体微缺失、Klinefelter综合征),CRISPR-Cas9等基因编辑技术可修复突变基因,结合干细胞移植恢复生精功能。
研究进展与临床案例
动物实验成功案例
2016年,中国科学家利用小鼠ESCs培育出功能性精子,成功生育健康后代。
2021年,日本团队将人类iPSCs分化为原始生殖细胞(PGCs),为人工精子提供可能。
初步临床试验
2017年,伊朗一项研究对NOA患者注射睾丸内MSCs,部分患者精液中重新出现精子。
2023年,美国启动基于SSCs移植的I期临床试验,目标为恢复生精功能。
结论
干细胞治疗为无精症患者提供了新的希望,尤其是非梗阻性无精症患者。然而,安全性、有效性及伦理问题仍需严格评估,以确保这项技术真正造福不育症患者。