日本研究人员成功地设计了iPSCs来分泌一种修饰的酶mNAGA,并在体外和小鼠模型中恢复了酶活性,为法布里病等疾病的再生医学开辟了新的途径。
研究人员通过使用诱导多能干细胞(iPSCs)在再生医学领域取得了重大进展。这些细胞来源于健康个体,在各种临床试验中显示出巨大的潜力。然而,最近的一项研究表明,使用iPSCs的移植疗法可以通过基因改造进一步增强。
在一项开创性的概念验证实验中,来自日本东京都立医学科学研究所的科学家利用法布里病小鼠模型探索iPSCs基因修饰的可能性。法布里病是一种遗传性疾病,由一种叫做α-半乳糖苷酶A(GLA)的酶缺乏引起,这种酶会导致体内有害物质的积累。为了解决这个问题,研究人员之前开发了一种修饰的酶,称为修饰的α-N-乙酰半乳糖苷酶(mNAGA),该酶有望治愈法布里病。
该团队开始进行这项研究,以研究通过基因组编辑分泌mNAGA的iPSCs是否可以在体内提供缺失的GLA活性。为了实现这一目标,他们采用TALEN介导的敲入技术,将mNAGA分泌引入称为AAVS1位点的安全港位点的iPSC中。此外,他们还使用CRISPR-Cas9来破坏iPSCs中的内源性GLA基因,旨在消除患者可能的免疫原性反应。
涉及工程化iPSCs与法布里病模型心肌细胞和成纤维细胞共培养的体外实验显示出有希望的结果。表达mNAGA的iPSCs成功地恢复了这些细胞中的GLA活性,有效地解决了这一缺陷。
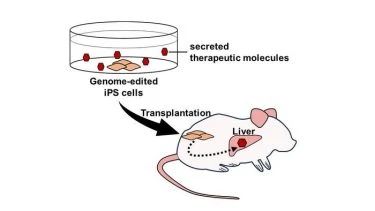
展望未来,该团队通过将分泌mNAGA的iPSC移植到法布里病模型小鼠的睾丸中进行了体内实验。7 至 8 周后,在肝脏中观察到 GLA 活性显着改善,而在心脏、肾脏或血浆中未观察到恢复。虽然肝脏中有害物质的水平,称为球三糖基神经酰胺 (Gb3) 和球三糖鞘氨醇 (Lyso-Gb3),没有降低,但确定移植的 iPSC 分泌的有限量的 mNAGA 不足以达到这种效果。
尽管目前存在局限性,但该研究强调了进一步发展的潜力。研究人员认为,通过基因组编辑技术增加分泌的mNAGA的数量可能是未来的可能性。此外,他们建议将mNAGA直接递送至需要GLA活性的特定器官和组织。例如,移植源自分泌mNAGA的iPSC的心肌细胞片可以直接将治疗分子输送到心脏。此外,该研究表明,该策略可以应用于法布里病以外的其他疾病。
这项研究证明了使用基因组编辑的iPSCs进行细胞治疗的潜力,这些iPSCs可以分泌治疗分子。这些工程化的iPSC不仅为细胞移植提供了资源,而且还是一种很有前途的药物递送系统。尽管需要进一步的研究和进步,但这些发现为再生医学的未来突破铺平了道路,并为法布里病等遗传性疾病患者提供了希望。
-END-
素材源于网络,内容有改动
版权归原作者所有,侵删!

