免疫疗法彻底改变了癌症治疗,嵌合抗原受体 (CAR)-T 细胞疗法已成为有前景的癌症免疫疗法。CAR-T 细胞是基因工程 T 细胞,可产生靶向癌细胞上特定抗原的人工 T 细胞受体。目前,有 六种 FDA 批准的 CAR-T 疗法. 所有这些都被批准用于治疗血癌。Kymriah 是 首个获得 FDA 批准的 CAR-T 细胞疗法,用于治疗急性淋巴细胞白血病(ALL)。
然而,尽管它们的临床疗效很好,CAR-T细胞仍然具有局限性、具有挑战性,限制之一是治疗后靶抗原的丢失。这使得 CAR-T 细胞效果大大降低,因为它们依赖于抗原来发挥功效。CAR-T 细胞疗法也与高毒性相关,例如细胞因子释放综合征和免疫效应细胞相关的神经毒性综合征,这可能会危及生命。靶向脱瘤毒性是另一个主要问题,因为 CAR-T 细胞识别的靶标是最常见的肿瘤相关抗原,这些抗原也在健康组织中表达。
由于其独特的特性,自然杀伤 (NK) 细胞已被确定为基于 CAR 细胞免疫疗法的最有希望的候选者。NK 细胞是细胞毒性杀伤细胞,通过先天性和适应性抗肿瘤活性靶向肿瘤细胞。
CAR-NK细胞 与 CAR-T 细胞相比有几个优势。由于 NK 细胞具有自发的细胞毒活性,它们可以通过 CAR 依赖性和 CAR 非依赖性途径杀死癌细胞,而 T 淋巴细胞仅通过 CAR 依赖性途径杀死它们的靶标。因此,在肿瘤抗原被下调的情况下,NK细胞仍然对肿瘤细胞有效。与 CAR-T 细胞的长期持久性不同,NK 细胞寿命短,因此不太可能维持靶向脱瘤毒性、细胞因子释放综合征和神经毒性。NK细胞可以从各种来源产生,例如脐带血、骨髓、人胚胎干细胞和诱导多能干细胞。这提供了作为现成 CAR-NK 疗法的可及性和可用性,这对于 CAR-T 细胞是不可能的,因为它通常来自自体来源。此外,由于 CAR-NK 是同种异体的,GVDH 的风险也显着降低。
由于这些独特的特点,CAR-NK 细胞免疫疗法可能会作为 CAR-T 疗法的替代品。然而,仍需要进一步的研究和临床试验来确保 CAR-NK 细胞的安全性。
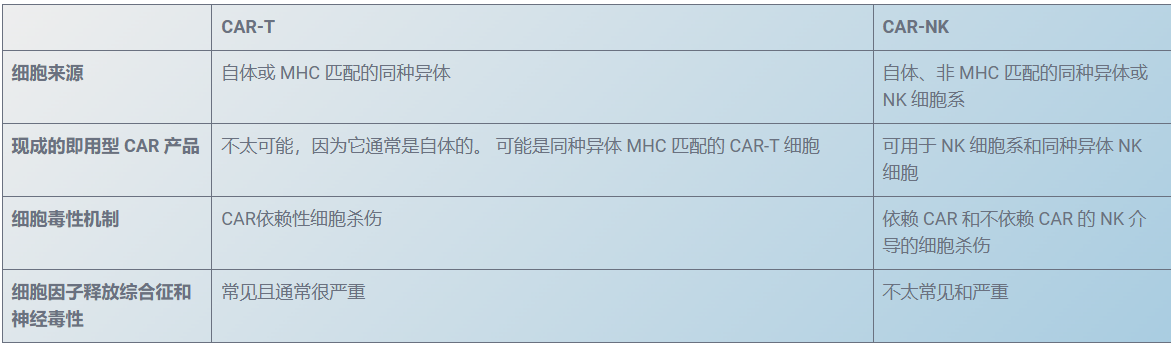
CAR-T 和 CAR-NK 癌细胞治疗的比较
GemPharmatech是转基因小鼠模型的领导者,已经创建了一系列小鼠模型来支持对 NK 细胞疗法的评估。NK 细胞的发育和功能需要细胞因子白细胞介素 15 (IL15) 体内。然而,小鼠 IL15 对人 NK 细胞的支持很差,因为它对人 IL15 受体的亲和力低。为了克服这个问题,GemPharmatech 在免疫缺陷小鼠模型 (NCG) 中敲入了人类 IL15 基因,以表达 hIL15 细胞因子—— NCG-hIL15 (T004886。与 NCG 对照相比,移植有 CD15+ 人类干细胞 (HSC) 的 NCG-hIL34 会产生显着更高水平的功能性人类 CD56+ NK 细胞(参见图 1 和图 2)。这种 NCG-hIL15 小鼠品系为研究人类 NK 细胞生物学和人类 NK 介导的癌症免疫疗法提供了一种新的小鼠模型 体内。
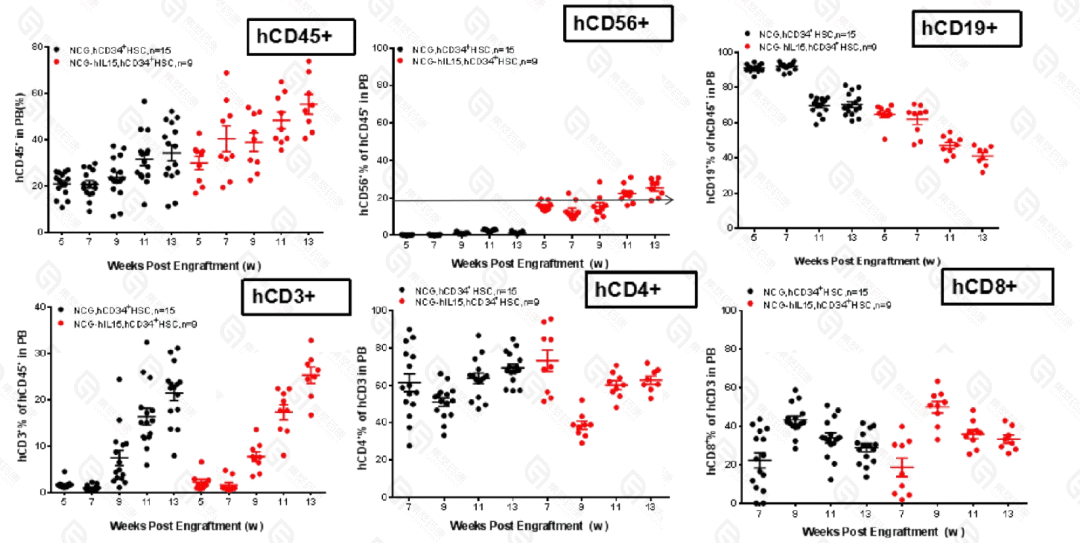
图 1:huHSC-NCG 和 huHSC-NCG-hIL15 小鼠的免疫表型
在植入后第 5、7、9、11 和 13 周收集外周血以表征免疫表型 huHSC-NCG 和 huHSC-NCG-hIL15 小鼠通过流式细胞术。与 huHSC-NCG 小鼠相比,CD56+ NK 细胞在 huHSC-NCG-hIL15 小鼠中表现出更高的重建水平。
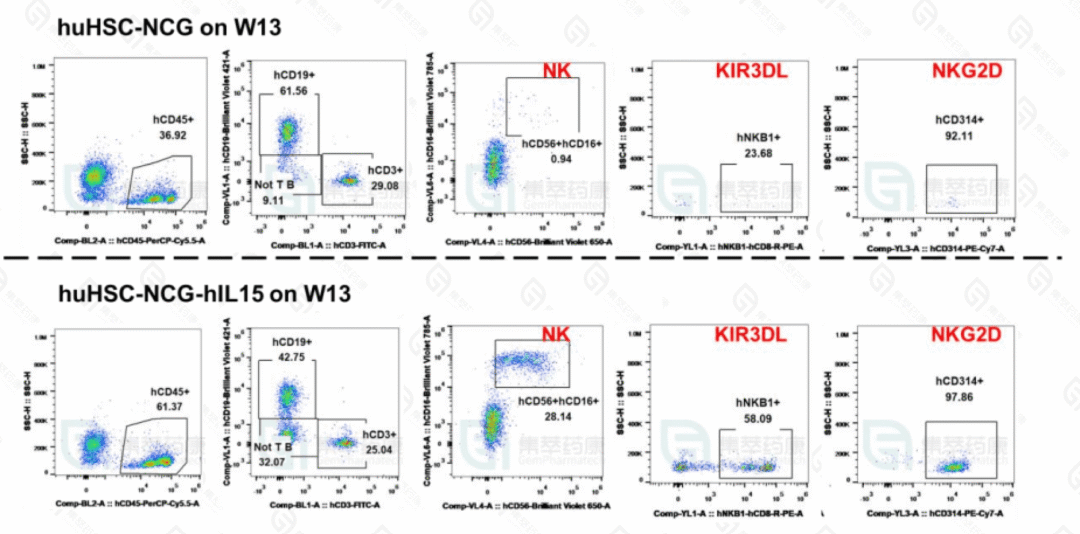
图2:典型NK细胞功能基因在huHSC-NCG和huHSC-NCG-hIL15小鼠中的表达
在移植后第 13 周收集外周血,以通过流式细胞术表征 huHSC-NCG 和 huHSC-NCG-hIL15 小鼠中的 NK 细胞功能基因。与huHSC-NCG相比,huHSC-NCG-hIL15小鼠NK细胞人源化重建水平显着提高,同时检测到功能蛋白KIR3DL和NKG2D。

